როგორ ვებრძვით ანტიბიოტიკების მიმართ რეზისტენტულობას — კვლევა ქართველი მეცნიერების მონაწილეობით

ფოტო: Wikimedia Commons
ბაქტერიულ ინფექციებთან ბრძოლის ყველაზე ეფექტიანი საშუალება, დღემდე, ანტიბიოტიკური პრეპარატებია. თუმცა, დროთა განმავლობაში, ანტიბიოტიკების ჭარბი გამოყენების გამო, გავრცელდა ისეთი პათოგენები, რომლებიც ანტიბიოტიკებისადმი რეზისტენტულობას, ანუ მდგრადობას იმუშავებენ. შესაბამისად, როცა ადამიანი ამა თუ იმ ინფექციის გადამტანია, სულ უფრო რთული ხდება მკურნალობა, რადგან ზუსტად ამ ბაქტერიების მხრიდან გამომუშავებული მდგრადობის გამო, ანტიბიოტიკები ეფექტურობას კარგავენ.
ანტიბიოტიკრეზისტენტულობა ერთგვარი დაჩქარებული ევოლუციაა. როცა ინფექციის საწყინააღმდეგოდ ანტიბიოტიკს ვხმარობთ, ის ყველაზე "სუსტ" ბაქტერიებს კლავს, თუმცა ეს "ძლიერ" ბაქტერიებს, რომლებმაც რეზისტენტულობა მუტაციით გამოიმუშავეს, გამრავლების შანსს აძლევს. შესაბამისად, საჯარო ჯანდაცვაში რეზისტენტული ბაქტერიები, დროთა განმავლობაში, სერიოზული პრობლემა გახდა და მეტიც, დროის გასვლასთან ერთად ეს პრობლემა სულ უფრო მწვავედ დადგება ჩვენს წინაშე.
რა თქმა უნდა, ამ პრობლემის ჯეროვანი შეფასების საფუძველზე, მეცნიერები რეზისტენტულობის წინააღმდეგ ბრძოლის გზების პოვნაზე უკვე მუშაობენ. არსებობს ბაქტერიული ინფექციების მკურნალობის ალტერნატიული საშუალებები, მაგალითად ბაქტერიოფაგებით მკურნალობა. ბაქტერიოფაგი ადამიანისთვის უვნებელი ვირუსია, რომელიც მხოლოდ ბაქტერიებს ანადგურებს, მათი გამოყენება ინფექციებთან ბრძოლაში სასარგებლოა ხოლმე და მკურნალობის ამ მეთოდს სერიოზული პოტენციალი აქვს.
ბაქტერიებთან გამკვლავების ერთ-ერთი მეთოდი, რომელიც ბოლო დროს მეცნიერებისთვის საინტერესოა "პეპტიდური" პრეპარატებია, რომლებიც ბაქტერიებს ასუსტებენ, ან კლავენ. თუმცა, ანტიბაქტერიული პრეპარატების შერჩევა და მომზადება რთული პროცესია. პრობლემის და პოტენციური გამოსავლის უკეთ გასაგებად, ჩვენ ბიოლოგ თორნიკე ნასრაშვილს ვესაუბრეთ, რომელიც ანტიბაქტერიული პეპტიდების კვლევაში იყო ჩართული.
პეპტიდები ბაქტერიების წინააღმდეგ

პეპტიდები ელექტრონულ მიკროსკოპში
ფოტო: Public Domain
კვლევა, რომლის შესახებაც თორნიკეს ვესაუბრე, საქართველოს აგრარულ უნივერსიტეტში ჩატარდა და უფრო მასშტაბური კვლევის ნაწილია, რომელიც წლებია მიმდინარეობს. სანამ დეტალებს განვიხილავდეთ, თორნიკეს ვთხოვე მარტივად აეხსნა პრობლემა, რომელზეც ის და მისი კოლეგები მუშაობდნენ.
თორნიკეს თქმით, ყველა ბაქტერია განსხვავებულია. ყველას თავისი "ხელწერა" აქვს. ანუ ზოგი ბაქტერია უფრო დამუხტულია, ზოგს უფრო სქელი კედელი აქვს, ზოგი ბევრად უფრო გაუმტარია და ა.შ.
პეპტიდი, თავის მხრივ, ამინომჟავების ჯაჭვს ეწოდება, საკმარისად დიდი პეპტიდური ჯაჭვი (50 ამინომჟავა ან მეტი) მცირე მოდიფიკაციით ცილა ხდება. ცილა კი ყველაფერი ცოცხალის ერთ-ერთი საშენი მასალაა, რომელიც დედამიწაზე სიცოცხლეს შესაძლებელს ხდის. ბაქტერიები, სხვა ორგანიზმების მსგავსად, ცილებისგან არიან აგებულნი, რომლებიც უამრავ ფუნქციას ასრულებენ.
როცა აღვნიშნეთ, რომ ყველა ბაქტერიას თავისი "ხელწერა" აქვს, ეს მეტწილად, სწორედ ბაქტერიული ცილების დამსახურებაა. ზუსტად იგივენაირად, როგორც სხვადასხვა სახლი სხვადასხვა საშენი მასალისგანაა აშენებული, ბაქტერიებიც სხვადასხვა ცილებისგან შედგებიან.
მეცნიერები, რომლებიც ანტიბიოტიკრეზისტენტულობას იკვლევენ, ცდილობენ იპოვონ ისეთ პეპტიდები, რომლებიც ბაქტერიულ უჯრედებს და მათ ცილებს მიემაგრებიან და პირველად თავდაცვას, ბაქტერიულ კედელს მოანგრევენ ან შეასუსტებენ.
იმის მიხედვით, თუ როგორია ბაქტერიის კედელი, შეგვიძლია გამოვყოთ გრამ დადებითი და გრამ უარყოფითი ბაქტერიები. გრამ უარყოფით ბაქტერიებს გარე ცხიმოვანი მემბრანა აქვთ, ხოლო გრამ დადებით ბაქტერიებს სქელი პეპტიდოგლიკანის შრე.
მთავარი აქ ისაა, რომ ძირითადად, ორი ტიპის ბაქტერია არსებობს (გრამ დადებითი და უარყოფითი) და მეცნიერებს აინტერესებთ, როგორ შეიძლება მათი თავდაცვის კედლის გარღვევა პეპტიდებით.
in Silico, ანუ კომპიუტერული მოდელირებიდან ექსპერიმენტებამდე

ფოტო: Abbas Salvaty
იმის გამო, რომ ბაქტერიულ ინფექციებთან ბრძოლა მსოფლიოში მუდმივად მიმდინარეობს, არსებობს ყველასთვის ხელმისაწვდომი მონაცემთა ბაზები, სადაც სხვადასხვა ბაქტერიების ნიშან-თვისებებია შენახული.
ანტიბაქტერიული პეპტიდების მოძიების პროცესი შემდეგნაირია: თავდაპირველად, მეცნიერები იძიებენ მათთვის საინტერესო ბაქტერიის ნიშანთვისებებს, შემდგომ კი ეძებენ ისეთ პეპტიდებს, რომლებიც ამ ბაქტერიებს მიესადაგება. პეპტიდების და ცილების ურთიერთქმედება ფაზლს წააგავს.
თავიდან ბაქტერიების შესაბამისი პეპტიდების ძიება in silico მოდელირებით სცადეს. ეს ნიშნავს, რომ მეცნეირებმა კომპიუტერული მოდელი შექმნეს, რომელიც კონკრეტულ ბაქტერიებს, კონკრეტული ამინომჟავური თანმიმდევრობის ცილებს მიუსადაგებდა.
კომპიუტერული მოდელირებით ისეთი პეპტიდების გენერირებაა შესაძლებელი, რომელიც ბუნებაში არ გვხვდება, მაგრამ მათი ხელოვნური სინთეზი შეგვიძლია.
მას შემდეგ, რაც მეცნიერებმა in silico მოდელირებით სხვადასხვა ბაქტერიებისთვის საუკეთსო კანდიდატი პეპტიდები შეარჩიეს, საჭირო გახდა ამ პეპტიდების რეალურ გარემოში გამოცდა.
აღსანიშნავია, რომ ზემოხსენებული in silico მოდელირება, ანუ კომპიუტერული მოდელი, რომელიც ბაქტერიების ანტიმიკრობულ პეპტიდებს უსადაგებს, მანქანური დასწავლის მეთოდის გამოყენებით მუშაობს. თორნიკეს თქმით:
"ჩატარებული ექსპერიმენტების შედეგები, კომპიუტერული მოდელისთვის კარგ უკუკავშირს იძლევა, შესაბამისად, ყოველ ახალ ექსპერიმენტზე, პროგრამა უფრო დახვეწილი ხდება და უფრო ეფექტიანად მუშაობს".
in Vitro ტესტები და შედეგები
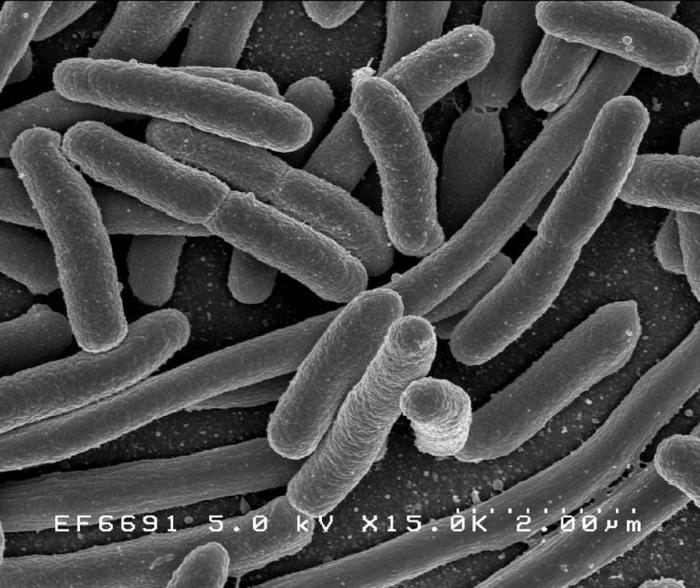
E.Coli ელექტრონულ მიკროსკოპში
ფოტო: Public Domain
მას შემდეგ, რაც საუკეთესო კანდიდატი პეპტიდები შეირჩა, მეცნიერებმა გადაწყვიტეს, რომ თავიდან ეს პეპტიდები მხოლოდ გრამ უარყოფით ბაქტერიებზე გამოეცადათ.
"გადაწყდა, რომ თავიდან მხოლოდ გრამ უარყოფით ბაქტერიებზე, E.Coli-ზე და სტაფილოკოკზე ვიმუშავებდით", — ამბობს თორნიკე.
დასინთეზირებული პეპტიდები L-ამინომჟავებისგან შედგებოდნენ (L და D ამინომჟავების ფორმებია). "ასეთი ამინომჟავური თანმიმდევრობები იმიტომ შევარჩიეთ, რომ D ამინომჟავები ადამიანის ორგანიზმში არ მოიპოვება".
in Vitro ტესტებს გიორგი ზაალიშვილი ხელმძღვანელობდა. მეცნიერების მთავარი მიზანი ანტიმიკრობული პეპტიდების მინიმალური კონცენტრაციის პოვნა იყო, რომელიც ბაქტერიების მოქმედებას შეზღუდავდა.
ანტიმიკრობული პეპტიდებისა და ბაქტერიების ურთიერთქმედების შესწავლა საკმაოდ ხანგრძლივი პროცესი გამოდგა, თუმცა, მეცნიერების შრომა დაფასდა, როცა აღმოჩნდა, რომ მათ მიერ შერჩეული პეპტიდები, გრამ უარყოფით ბაქტერიებზე, 80-90%-იანი ეფექტიანობით მუშაობდნენ.

ანტიმიკრობული პეპტიდების ინფექციასთან ბრძოლაში გამოყენებისას მნიშვნელოვანია, რომ პეპტიდებმა ისე იმოქმედონ ბაქტერიებზე, რომ ადამიანის ჯანმრთელი უჯრედები არ დააზიანონ. მიუხედავად იმისა, რომ ეს ექსპერიმენტი ბაქტერიულ კულტურებზე მიმდინარეობდა და არა ინფიცირებულ ცოცხალ ორგანიზმებზე, ეს გარემოება გათვალისწინებული იყო.
"ცნობილია, რომ ანტიმიკრობული პეპტიდები [ბაქტერიის] მემბრანასთან ურთიერთქმედებენ, თუმცა რა გზებით ახერხებენ ამას, არ ვიცით", — ამბობს თორნიკე.
სინთეზირებული პეპტიდების ეფექტიანობას (ანუ რამდენად კარგად შეაჩერა ბაქტერიის მოქმედება) მკვლევრები ფლუროსცენტული მიკროსკოპიით დააკვირდნენ. ასეთ დროს, იყენებენ სპეციალურ საღებავს, რომელიც ბაქტერიის მემბრანაში მხოლოდ მაშინ აღწევს, თუ მემბრანის სტრუქტურა დაზიანებულია. შესაბამისად, თუ საღებავი შეაღწევდა და ეს მიკროსკოპში გამოჩნდებოდა, ესეიგი პეპტიდმა მემბრანა გაარღვია.
მეორე მხრივ, საღებავის ხილვადობა ნაკლები იქნებოდა, თუ პეპტიდმა ბაქტერიის შიდა სისტემები გაანადგურა. ანტიმიკრობული პეპტიდების მოქმედების გასაგებად, მეცნიერებმა ორი პეპტიდი გამოცადეს. ერთ შემთხვევაში აღინიშნებოდა მემბრანის რღვევა, მეორე შემთხვევაში კი შიდა სისტემების განადგურება. რაც ნიშნავს, რომ
ანტიბიოტიკებისადმი რეზისტენტულობა სერიოზული პრობლემაა

ფოტო: Getty Images
ანტიბიოტიკების აღმოჩენა და მათი მასობრივი წარმოება კაცობრიობის ერთ-ერთი უმნიშვნელოვანესი მიღწევაა. თუმცა, იმის გამო, რომ ანტიბიოტიკებს ხშირად არც ისე მიზანშეწონილად იყენებენ, საჯარო კეთილდღეობას და ჯანმრთელობას საფრთხე ემუქრება.
ანტიბიოტიკების ჭარბი და უმისამართო გამოყენება, ბაქტერიებს სწრაფი ევოლუციის საშუალებას აძლევს. თუ ასე გაგრძელდა, შესაძლოა "პოსტ-ანტიბიოტურ" ეპოქაში შევაბიჯოთ, სადაც მარტივი ინფექციები მასშტაბური ზიანის მომტანი იქნება.
საიამოვნო სანახავია, რომ მიმდინარეობს კვლევები, მათ შორის საქართველოში, სადაც მეცნიერები ცდილობენ, რომ ჯანდაცვის ძალიან სერიოზულ გამოწვევებს გაუმკლავდნენ. თორნიკეს თქმით, ზემოხსენებული ექსპერიმენტი მეცნერებს საშუალებას აძლევს, რომ ანტიმიკრობული პეპტიდები მარტივად შეირჩეს, რომელთა იმპლემენტაცია სამკურნალო პრაქტიკაში ძალიან სასარგებლო შეიძლება გამოდგეს.
თუ სტატიაში განხილული თემა და ზოგადად, მეცნიერებისა და ტექნოლოგიების სფერო შენთვის საინტერესოა, შემოგვიერთდი ჯგუფში – შემდეგი ჯგუფი.











კომენტარები